Chi5 - Lampe de Davy
Fonction
Avant l'emploi de lampes électriques, on s'éclairait dans les mines de charbon avec des lampes à flamme, mais celles-ci provoquaient de terribles "coups de grisou". Tout en éclairant avec une flamme, la lampe Davy devait, en principe, éviter ces catastrophes. Pour cela la flamme de la lampe est totalement entourée par une toile métallique.
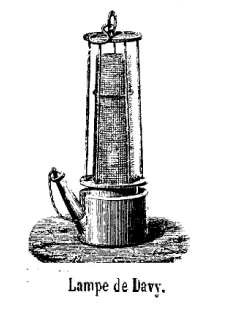
Description
Rappelons tout d'abord que le « grisou » est un mélange gazeux contenant essentiellement du méthane (CH4), combustible, libéré par l'abattage du charbon et qu'il forme avec l'air un mélange explosif.
Une flamme est un gaz en mouvement, rendu lumineux, donc visible, lorsqu'une réaction chimique (une oxydation le plus souvent) se produit en son sein et dégage de la chaleur. Au-dessous d'une certaine température (seuil), les molécules du mélange gazeux se heurtent sans se briser (chocs élastiques). À partir d'une température suffisante, supérieure au seuil (plus grande énergie cinétique des molécules), les chocs brisent les molécules dont les atomes se réarrangent pour former des molécules nouvelles :
CH4 + 2O2 → CO2 +2H2O.
Les molécules sont excitées : leur retour à un état d'énergie plus basse s'accompagne de l'émission de photons d'où la luminosité de la flamme. La flamme se maintient si l'énergie produite par la réaction chimique compense les pertes de chaleur (rayonnement, conduction...)
On éteint une flamme en supprimant ou en réduisant soit le flux de carburant gazeux, soit le flux d'oxygène (couvrir la flamme d'une bougie avec un cône éteignoir). Mais on peut aussi éteindre une flamme en augmentant les pertes de chaleur pour abaisser la température au-dessous du seuil : la réaction chimique s'arrête. Un fort débit d'air y suffit (souffler une bougie). On peut aussi faire l'expérience suivante : couvrons une flamme avec une toile tissée avec des fils métalliques peu serrés, bons conducteurs de la chaleur. Les gaz de la flamme, visibles sous la toile, sont fortement refroidis à la traversée de celle-ci et ne réagissent plus ; ils ne sont donc plus visibles au-dessus de la toile. Une allumette présentée au-dessus de la toile métallique peut réamorcer la réaction chimique au-dessus de la toile et rendre ainsi visibles les gaz qui l'ont traversée.

Revenons au fonctionnement de la lampe de Davy. Supposons que le mineur muni de sa lampe pénètre dans une zone où l'air contient un gaz combustible : celui-ci entre dans la lampe, vient au contact de la flamme qui déclenche à l'intérieur de la lampe un « mini coup de grisou » ; mais les gaz produits, fortement refroidis en traversant la toile métallique de l'intérieur vers l'extérieur, ne peuvent servir d'amorce à une combustion externe (encore faut-il qu'il n'y ait pas de trous dans la toile et qu'il n'y ait pas de particules incandescentes sur la toile). La lampe sert ainsi de détecteur de grisou : il convient alors d'évacuer la région et d'éviter toute étincelle et a fortiori de ne pas utiliser d'allumettes.
Histoire
Un vieux registre nous apprend qu'une "lampe de sûreté de Combes", appartenant à la collection a été réparée en 1895. Le polytechnicien et académicien des sciences Charles Pierre Mathieu Combes (1801-1872) a enseigné à l'école des mines de Saint-Étienne. L'art des mines lui est redevable de nombreux progrès. Faut-il rendre à César … ?
Le chimiste anglais, Sir Humphry Davy (1778-1829) est le découvreur de « l'action hilarante » du protoxyde d'azote (N2O), la découverte du potassium et sodium, et l'affirmation que le chlore est un corps simple ; il a également expérimenté l'action de « la vapeur de charbon » sur sa propre personne. On lui doit la construction d'une pile différente et plus puissante que celle de Volta et par l'occasion la découverte des premiers phénomènes électrochimiques, ainsi que la lampe des mineurs dont il est question ici.
Il est élu membre de la Royal Society en 1803 et correspondant de l'Académie des Sciences en 1818 ; il a participé aux fouilles d'Herculanum (1827-1828).